徕卡神经外科手术可视化AR荧光解决方案,通过FDA批准
发布时间:2018-09-26 10:30 来源: 青亭网
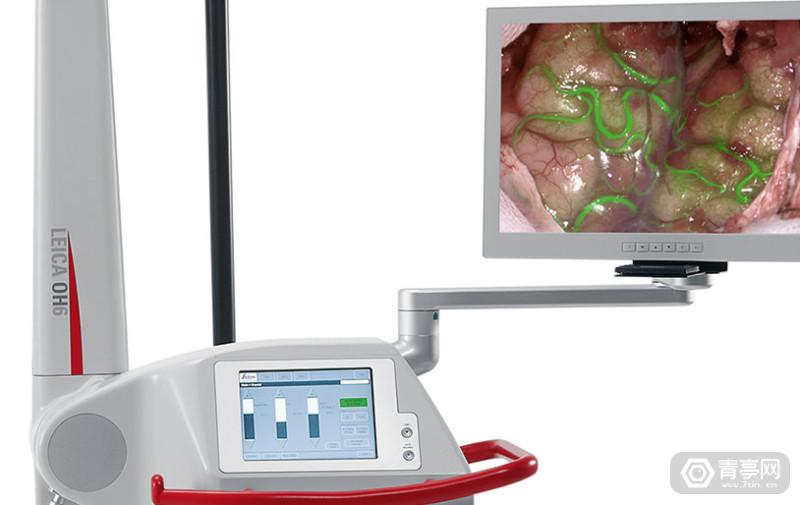
近日,徕卡显微系统公司获得了美国食品及药物管理局批准的510(k)文件,意味着其应用于血管神经手术的外科AR荧光技术GLOW800即将进入上市阶段。据悉,这项技术使用吲哚菁绿(IGG),可帮助外科医生以完整的深度知觉观测到大脑的自然颜色和实时的血液流动。在进行血管神经手术过程中,GLOW800 AR解决方案可协助外科医生观察到手术区域的完整生理结构和技能,更好地决策和判断。
注:510(k)文件:向FDA递交的上市前申请文件。
吲哚菁绿:诊断用药,用来检查肝脏功能和干有效流量的染料药。
徕卡显微系统公司总裁Markus Lusser表示:“过去十年来徕卡显微系统在使用荧光成像技术与外科医生合作方面一直是领航者,GLOW800以及未来基于GLOW AR平台的更多技术将会帮助外科医生完成患者人生的神经外科介入手术,因为我们会为他们提供市面上最好的可视化解决方案。”
GLOW800 AR荧光技术最初亮相于去年10月,是徕卡显微系统推出的第一批基于GLOW AR平台的成像方案之一,可完全兼容徕卡显微系统在今年初推出的ARveo数字AR显微镜。美国食品及药品管理局批准了GLOW800的510(k)文件后,ARveo的美国用户将会在手术室体验到完整的AR可视化技术,这将大大改变传统手术的方式。
声明:本站在转载文章时均注明来源出处,转载目的在于传递更多信息,未用于商业用途。如因本站的文章、图片等在内容、版权或其它方面存在问题或异议,请与本站联系(电话:020-37784831,邮箱:edit@fly-tech.com.cn),本站将作妥善处理。
推荐阅读